خوردگی فلزات
خوردگی ، ( Corrosion ) ، اثر تخریبی محیط بر فلزات و آلیاژها میباشد. خوردگی ، پدیدهای خودبهخودی است و همه مردم در زندگی روزمره خود ، از بدو پیدایش فلزات با آن روبرو هستند. در اثر پدیده خودبهخودی ، فلز از درجه اکسیداسیون صفر تبدیل به گونهای با درجه اکسیداسیون بالا میشود.
تخریب فلزات با عوامل غیر خوردگی
فلزات در اثر اصطکاک ، سایش و نیروهای وارده دچار تخریب میشوند که تحت عنوان خوردگی مورد نظر ما نیست.فرایند خودبهخودی و فرایند غیرخودبهخودی
خوردگی یک فرایند خودبخودی است، یعنی به زبان ترمودینامیکی در جهتی پیش میرود که به حالت پایدار برسد. البته M+n میتواند به حالتهای مختلف گونههای فلزی با اجزای مختلف ظاهر شود. اگر آهن را در اتمسفر هوا قرار دهیم، زنگ میزند که یک نوع خوردگی و پدیدهای خودبهخودی است. انواع مواد هیدروکسیدی و اکسیدی نیز میتوانند محصولات جامد خوردگی باشند که همگی گونه فلزی هستند. پس در اثر خوردگی فلزات در یک محیط که پدیدهای خودبهخودی است، اشکال مختلف آن ظاهر میشود.بندرت میتوان فلز را بصورت فلزی و عنصری در محیط پیدا کرد و اغلب بصورت ترکیب در کانیها و بصورت کلریدها و سولفیدها و غیره یافت میشوند و ما آنها را بازیابی میکنیم. به عبارت دیگر ، با استفاده از روشهای مختلف ، فلزات را از آن ترکیبات خارج میکنند. یکی از این روشها ، روش احیای فلزات است. بعنوان مثال ، برای بازیابی مس از ترکیبات آن ، فلز را بصورت سولفات مس از ترکیبات آن خارج میکنیم یا اینکه آلومینیوم موجود در طبیعت را با روشهای شیمیایی تبدیل به اکسید آلومینیوم میکنند و سپس با روشهای الکترولیز میتوانند آن را احیا کنند.
برای تمام این روشها ، نیاز به صرف انرژی است که یک روش و فرایند غیرخودبهخودی است و یک فرایند غیرخودبهخودی هزینه و مواد ویژهای نیاز دارد. از طرف دیگر ، هر فرایند غیر خودبهخودی درصدد است که به حالت اولیه خود بازگردد، چرا که بازگشت به حالت اولیه یک مسیر خودبهخودی است. پس فلزات استخراج شده میل دارند به ذات اصلی خود باز گردند.
در جامعه منابع فلزات محدود است و مسیر برگشت طوری نیست که دوباره آنها را بازگرداند. وقتی فلزی را در اسید حل میکنیم و یا در و پنجره دچار خوردگی میشوند، دیگر قابل بازیابی نیستند. پس خوردگی یک پدیده مضر و ضربه زننده به اقتصاد است.
جنبههای اقتصادی فرایند خوردگی
برآوردی که در مورد ضررهای خوردگی انجام گرفته، نشان میدهد سالانه هزینه تحمیل شده از سوی خوردگی ، بالغ بر 5 میلیارد دلار است. بیشترین ضررهای خوردگی ، هزینههایی است که برای جلوگیری از خوردگی تحمیل میشود.
پوششهای رنگها و جلاها
سادهترین راه مبارزه با خوردگی ، اعمال یک لایه رنگ است. با استفاده از رنگها بصورت آستر و رویه ، میتوان ارتباط فلزات را با محیط تا اندازهای قطع کرد و در نتیجه موجب محافظت تاسیسات فلزی شد. به روشهای سادهای میتوان رنگها را بروی فلزات ثابت کرد که میتوان روش پاششی را نام برد. به کمک روشهای رنگدهی ، میتوان ضخامت معینی از رنگها را روی تاسیسات فلزی قرار داد.
آخرین پدیده در صنایع رنگ سازی ساخت رنگهای الکتروستاتیک است که به میدان الکتریکی پاسخ میدهند و به این ترتیب میتوان از پراکندگی و تلف شدن رنگ جلوگیری کرد.
پوششهای فسفاتی و کروماتی
این پوششها که پوششهای تبدیلی نامیده میشوند، پوششهایی هستند که از خود فلز ایجاد میشوند. فسفاتها و کروماتها نامحلولاند. با استفاده از محلولهای معینی مثل اسید سولفوریک با مقدار معینی از نمکهای فسفات ، قسمت سطحی قطعات فلزی را تبدیل به فسفات یا کرومات آن فلز میکنند و در نتیجه ، به سطح قطعه فلز چسبیده و بعنوان پوششهای محافظ در محیطهای خنثی میتوانند کارایی داشته باشند.
این پوششها بیشتر به این دلیل فراهم میشوند که از روی آنها بتوان پوششهای رنگ را بر روی قطعات فلزی بکار برد. پس پوششهای فسفاتی ، کروماتی ، بعنوان آستر نیز در قطعات صنعتی میتوانند عمل کنند؛ چرا که وجود این پوشش ، ارتباط رنگ با قطعه را محکمتر میسازد. رنگ کم و بیش دارای تحلخل است و اگر خوب فراهم نشود، نمیتواند از خوردگی جلوگیری کند.
پوششهای اکسید فلزات
اکسید برخی فلزات بر روی خود فلزات ، از خوردگی جلوگیری میکند. بعنوان مثال ، میتوان تحت عوامل کنترل شده ، لایهای از اکسید آلومینیوم بر روی آلومینیوم نشاند. اکسید آلومینیوم رنگ خوبی دارد و اکسید آن به سطح فلز میچسبد و باعث میشود که اتمسفر به آن اثر نکرده و مقاومت خوبی در مقابل خوردگی داشته باشد. همچنین اکسید آلومینیوم رنگپذیر است و میتوان با الکترولیز و غوطهوری ، آن را رنگ کرد. اکسید آلومینیوم دارای تخلخل و حفرههای شش وجهی است که با الکترولیز ، رنگ در این حفرهها قرار میگیرد.
همچنین با پدیده الکترولیز ، آهن را به اکسید آهن سیاه رنگ (البته بصورت کنترل شده) تبدیل میکنند که مقاوم در برابر خوردگی است که به آن "سیاهکاری آهن یا فولاد" میگویند که در قطعات یدکی ماشین دیده میشود.
پوششهای گالوانیزه
گالوانیزه کردن (Galvanizing) ، پوشش دادن آهن و فولاد با روی است. گالوانیزه ، بطرق مختلف انجام میگیرد که یکی از این طرق ، آبکاری با برق است. در آبکاری با برق ، قطعهای که میخواهیم گالوانیزه کنیم، کاتد الکترولیز را تشکیل میدهد و فلز روی در آند قرار میگیرد. یکی دیگر از روشهای گالوانیزه ، استفاده از فلز مذاب یا روی مذاب است. روی دارای نقطه ذوب پایینی است.
در گالوانیزه با روی مذاب آن را بصورت مذاب در حمام مورد استفاده قرار میدهند و با استفاده از غوطهور سازی فلز در روی مذاب ، لایهای از روی در سطح فلز تشکیل میشود که به این پدیده ، غوطهوری داغ (Hot dip galvanizing) میگویند. لولههای گالوانیزه در ساخت قطعات مختلف ، در لوله کشی منازل و آبرسانی و ... مورد استفاده قرار میگیرند.
پوششهای قلع
قلع از فلزاتی است که ذاتا براحتی اکسید میشود و از طریق ایجاد اکسید در مقابل اتمسفر مقاوم میشود و در محیطهای بسیار خورنده مثل اسیدها و نمکها و ... بخوبی پایداری میکند. به همین دلیل در موارد حساس که خوردگی قابل کنترل نیست، از قطعات قلع یا پوششهای قلع استفاده میشود. مصرف زیاد این نوع پوششها ، در صنعت کنسروسازی میباشد که بر روی ظروف آهنی این پوششها را قرار میدهند.
پوششهای کادمیم
این پوششها بر روی فولاد از طریق آبگیری انجام میگیرد. معمولا پیچ و مهرههای فولادی با این فلز ، روکش داده میشوند.
فولاد زنگنزن
این نوع فولاد ، جزو فلزات بسیار مقاوم در برابر خوردگی است و در صنایع شیر آلات مورد استفاده قرار میگیرد. این نوع فولاد ، آلیاژ فولاد با کروم میباشد و گاهی نیکل نیز به این آلیاژ اضافه میشود.
این مطلب در تاریخ: پنج شنبه 28 آذر 1392 ساعت: 1:38 منتشر شده است












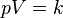
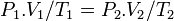
 فشار گاز ایدهآل در قبل از فرآیند
فشار گاز ایدهآل در قبل از فرآیند حجم گاز ایدهآل در قبل از فرآیند
حجم گاز ایدهآل در قبل از فرآیند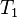 دمای گاز ایدهآل در قبل از فرآیند
دمای گاز ایدهآل در قبل از فرآیند فشار گاز ایدهآل در بعد از فرآیند
فشار گاز ایدهآل در بعد از فرآیند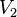 حجم گاز ایدهآل در بعد از فرآیند
حجم گاز ایدهآل در بعد از فرآیند دمای گاز ایدهآل در بعد از فرآیند
دمای گاز ایدهآل در بعد از فرآیند



